图片由JNM
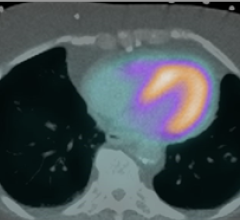
2021年6月28日,美国食品和药物管理局(FDA)批准了一项新的检测显像剂前列腺癌,提供一个更有效的成像方法检测癌症的扩散到身体的其他部位。Piflufolastat f - 18注射是第一个氟化前列腺特异性膜抗原(PSMA)代理FDA批准的也是第一个商用PSMA PET显像剂。
代理被批准PET成像前列腺癌患者的PSMA-positive病变
- 疑似候选人首次明确的治疗或转移
- 疑似复发基于升高血清前列腺特异性抗原(PSA)水平。
“我们认为今天的批准是改变男性面对前列腺癌,”杰米Bearse说,首席执行官零——前列腺癌的结束,一个病人。“有一个诊断工具,允许医生看到疑似转移或复发性前列腺癌前,在身体的任何地方,是向前迈出的重要一步,将对患者的生活有巨大的影响。”
代理,最初叫道18F-DCFPyL,是由马丁博,医学博士,博士,核医学和分子成像主任约翰·霍普金斯大学医学院的。新药申请代理提起2020年9月和12月FDA授予优先审查的。研究支持代理批准来自两个关键的多中心研究秃鹰学习和鱼鹰研究。
代理是由Lantheus制造Pylarify注入和将在美国广泛使用。
更多信息:www.snmmi.org
有关前列腺显像剂信息:
在解剖区域形成PSMA-Targeted放射性示踪剂的转移性前列腺癌

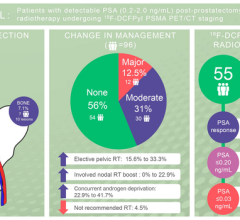
 2022年9月8日
2022年9月8日