盖蒂图片社
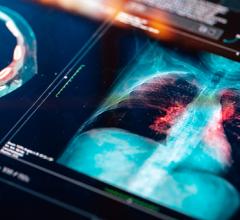
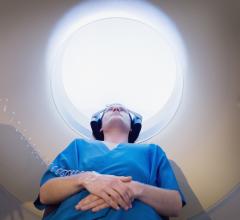
2020年12月4日-今天美国食品和药物管理局(FDA)发布了一项立即生效的指导,2019冠状病毒病突发公共卫生事件期间《乳房x光检查质量标准法》质量标准执行政策.本指南提供了FDA的执行政策和一般考虑,以应对乳房x光检查设施面临的常见情况,由于新型冠状病毒肺炎突发公共卫生事件
FDA在保护美国免受新出现的传染病等威胁方面发挥着关键作用,包括2019冠状病毒病(COVID-19)大流行。FDA致力于提供及时的指导,以支持应对这一流行病的努力。
FDA发布本指南是为了提供FDA关于某些质量标准要求的执行政策1992年乳房x光检查质量标准法案(MQSA),并为在公共卫生紧急事件期间可能暂时停止进行乳房x光检查或可能继续进行乳房x光检查但在遵守某些质量标准要求方面面临困难的设施提供一般考虑。MQSA是的一部分美国法典第42篇————公共卫生和福利,并在FDA的规定中实施CFR第900部分.
本政策仅适用于卫生与公众服务部部长(HHS)于2020年1月31日宣布的与COVID-19有关的突发公共卫生事件期间,并于2020年1月27日生效,包括HHS部长根据《公共卫生服务法》(小服务法)第319(a)(2)条作出的任何续订。
鉴于此次公共卫生紧急事件,并如2020年3月25日联邦公报上题为“提供2019冠状病毒病相关指导文件的过程“本指南的实施没有事先征求公众意见,因为FDA已确定本指南的事先公众参与不可行或不合适(见《联邦食品、药物和化妆品法》(FD&C法)第701(h)(1)(C)条(21 U.S.C. 371(h)(1)(C))和21 CFR 10.115(g)(2)))。该指导文件正在立即执行,但仍需根据原子能机构的良好指导做法进行评论。


 2022年9月22日
2022年9月22日