盖蒂图片社
2022年3月23日——今天的美国食品和药物管理局(FDA)的批准177年陆- psma - 617——放射性药物疗法治疗转移性前列腺癌castration-resistant (mCRPC)- - -核医学学会和分子成像(SNMMI)庆祝核医学历史上最伟大的成功故事之一。发达国家经过多年的广泛研究,治疗已被证明死亡的风险降低38%,进展的风险减少60% mCRPC患者177年陆- psma - 617。
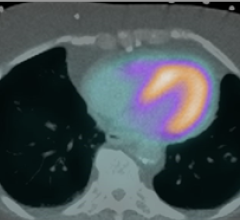
新疗法取决于使用的PET扫描识别和治疗转移性前列腺癌的患者表达PSMA(前列腺特异膜抗原)。“我们很高兴通过FDA批准这种转型,创新治疗前列腺癌晚期转移性阉割抵抗,“SNMMI总统说医学博士Richard l . Wahl FACNM。“我们很自豪的社会成员作出了显著贡献这个新的theranostic范式,以及所有的作者发表文章在这种疗法《核医学杂志》上。”
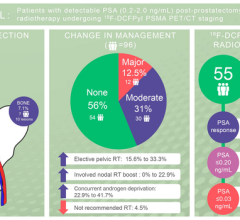
FDA授予重点审查177年陆- psma - 617在2021年9月基于积极的多中心三期的数据视觉研究中,测量总体存活率和无进展生存mCRPC患者疾病进展,尽管治疗。
这项工作的成功建立在先前的放射性药物疗法等177年Lu-DOTATATE,它提供了一个重要的临床效益患者神经内分泌肿瘤。SNMMI计划为医生和患者提供指导和支持177年陆- psma - 617变得可用。社会已更新其适当使用标准PSMA PET成像包括一个显示“评估资格为PSMA-targeted病人正在考虑放射性配体治疗”,被列为“适当”PSMA靶向治疗的可用性。此外,资源将被开发教育mCRPC病人对新疗法。
“FDA批准177年lu - psma - 617是证明了核医学创新者,与临床密切合作的同事在前列腺癌治疗领域,可以完成与他们的专长的独特组合基础生物学,放射化学,物理,和仪表,”Wahl指出。“放射性药物疗法的发展是迅速推进,我们完全相信将会有更多的是他们可以如此有效和有利于病人抗击癌症。”
前列腺癌是男性第二个最常见的癌症。超过268000例前列腺癌和预计大约有34500人死亡于2022年在美国。虽然局限性前列腺癌的5年生存率是近100%,mCRPC患者只有30%。
177年陆- psma - 617是由诺华公司制造。
更多信息:www.snmmi.org
前列腺癌相关内容:
视频:MRI-Linac GenesisCare和PET成像技术PSMA艾滋病治疗

 2022年9月14日
2022年9月14日